Giới thiệu CRISPR/Cas9
CRISPR/Cas9 là một công nghệ chỉnh sửa gene, công trình nghiên cứu của hai giáo sư Jennifer Doudna và Emmanuelle Charpentier được công bố lần đầu tiên vào năm 2012. Hiện nay, CRISPR/Cas9 là công nghệ chỉnh sửa gene đơn giản, linh hoạt và có độ chính xác cao được ứng dụng rộng rãi trên trong nông nghiệp, động vật, chuẩn đoán. Trong lĩnh vực y học và trị liệu, CRISPR/Cas9 đang được nghiên cứu trong việc sử dụng để điều trị cho người bị nhiễm HIV và một số nghiên cứu đang ứng dụng để điều trị sửa chữa các đột biến liên quan đến bệnh di truyền bao gồm: tiểu đường, ung thư.

Khái niệm, chức năng của hệ thống CRISPR/Cas ở vi khuẩn và lịch sử phát triển của kỹ thuật CRISPR/Cas9
CRISPR được viết tắt của những chữ cái đầu của cụm từ (Clustered Regularly Interspaced Short Palindromic Repeats )là một họ các trình tự DNA được tìm thấy trong bộ gene lần đầu tiên ở trong vi khuẩn và vi khuẩn cổ vào năm 1987 từ nhóm tác giả Ishino và cộng sự. Tuy nhiên, tại thời điểm đó chức năng và vai trò của các đoạn CRISPR vẫn chưa được làm rõ.
Đến năm 2007, nhóm tác giả Rodolphe Barrangou và cộng sự đã chứng minh chức năng của hệ thống CRISPR/Cas là một hệ thống miễn dịch đáp ứng tồn tại ở hầu hết các vi khuẩn và vi khuẩn cổ, ngăn chúng khỏi bị xâm nhiễm bởi virus và các yếu tố di truyền ngoại lai khác. Cấu trúc chung của một CRISPR bao gồm các mảng spacer lặp lại có thể được phiên mã tiếp thành CRISPR RNA (crRNA) và trans-activating CRISPR RNA (tracrRNA) và một gen CRISPR-associated được viết tắt cas có chức năng mã hóa protein Cas với chức năng endonuclease.
Khi sinh vật nhân sơ bị các yếu tố di truyền ngoại lai xâm nhiễm, các DNA ngoại lai có thể bị protein Cas cắt thành các đoạn ngắn. sau đó các đoạn DNA này sẽ được tích hợp vào các đoạn CRISPR dưới dạng các spacer mới. Một khi kẻ có sự xuất hiện của các yếu tố di truyền ngoại lại tương tự xâm nhiễm một lần nữa, crRNA sẽ nhanh chóng nhận biết và ghép đôi với DNA ngoại lai, điều này hướng dẫn protein Cas cắt các chuỗi mục tiêu của DNA ngoại lai, từ đó bảo vệ vật chủ.


Năm 2012, lần đầu tiên công nghệ CRISPR được ứng dụng làm kĩ thuật chỉnh sửa gen nhờ công trình nghiên cứu của nhóm tác giả Jennifer Doudna và Emmanuelle Charpentier tại trường đại học California. Trong nghiên cứu này nhóm tác giả đã đưa vào trong tế bào một phức hệ bao gồm enzyme Cas9 nuclease và một gRNA (guide RNA) tự thiết kế để cắt các đoạn DNA tại những vị trí mong muốn.
Phân loại của hệ thống CRISPR/Cas
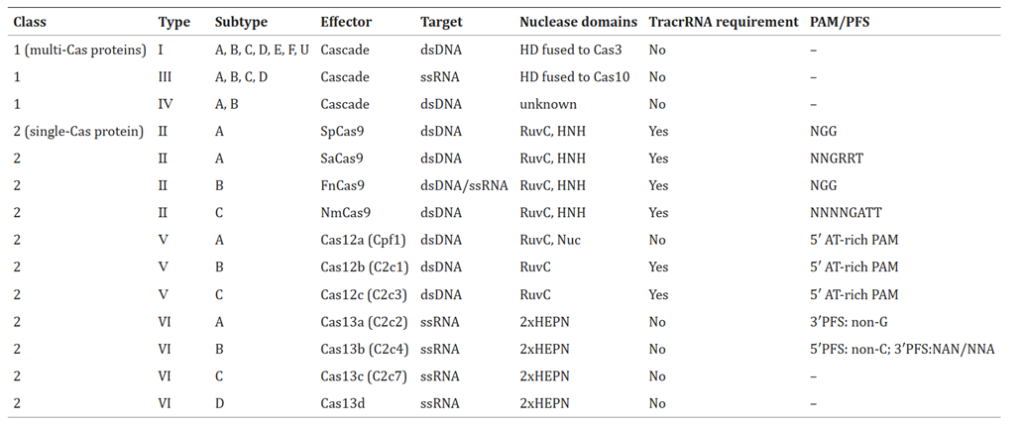
Hệ thống CRISPR/Cas có thể được phân thành 2 nhóm (nhóm I và nhóm II), 6 types (I đến VI) và một số types phụ. Việc phân loại, các thành viên đại diện và các đặc điểm điển hình của từng hệ thống CRISPR/Cas được tóm tắt trong hình 4.
Thành phần, nguyên lý hoạt động của hệ thống, công nghệ CRISPR/Cas9
Hệ thống CRISPR/Cas9 types II có nguồn gốc từ Streptococcus pyogenes (SpCas9) là một trong những types có các đặc điểm tốt và được sử dụng phổ biến nhất trong nhiều hệ thống CRISPR/Cas.
Thành phần chính của hệ thống CRISPR/Cas9 bao gồm enzyme Cas9 nuclease (Cas9 protein) và single-guide RNA (sgRNA). Protein Cas9 sở hữu hai miền nuclease, được đặt tên là HNH và RuvC, và mỗi miền sẽ cắt một chuỗi của chuỗi DNA mục tiêu. sgRNA là sự kết hợp đơn giản giữa crRNA và tracrRNA. Cas9 nuclease và sgRNA tạo thành phức hợp Cas9 ribonucleoprotein (RNP), có thể liên kết và phân tách mục tiêu DNA cụ thể.
Ngoài ra, để có thể hoạt động, hệ thống CRISPR còn yêu cầu một trình tự ngắn từ 2-5 nucleotides trên DNA đích được gọi là protospacer associated motif (PAM) ngay sau đoạn bổ sung của gRNA. Khi phức hợp Cas9 và gRNA bám vào trình tự đích, enzyme Cas9 sẽ dùng 2 tiểu phần HNH và RuVC của mình để cắt đoạn DNA trên cả 2 mạch tại vị trí nucleotide thứ 3-4 phía trước PAM.

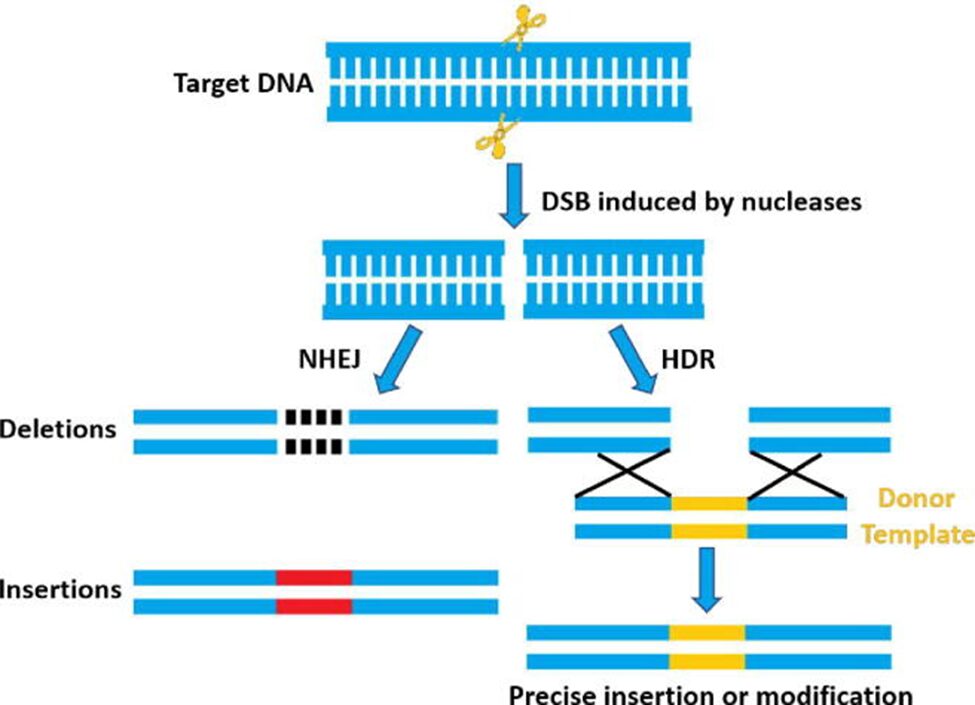
Theo cơ chế tự sửa chữa của tế bào, đoạn DNA sau khi bị cắt sẽ được sửa chữa lại theo 2 con đường bao gồm: con đường ghép nối không tương đồng (non-homologous end joing NHEJ) và con đường sửa chữa tái tổ hợp tương đồng (homology directed repair – HDR). Con đường sửa chữa NHEJ sẽ tạo ra các đột biến mất hoặc mất nucleotide, trong khi con đường sửa chữa HDR sử dụng template (khuôn mẫu) có trình tự tương đồng ở khớp nối nên bảo toàn được trình tự DNA.
Thông qua cơ chế cắt và nối DNA này các nhà khoa học có thể thêm, xoá, thay đổi trình tự DNA trong hệ gen. Trong hầu hết các điều kiện, NHEJ hiệu quả hơn HDR vì nó hoạt động trong khoảng 90% chu kỳ tế bào và không phụ thuộc vào khuôn mẫu tương đồng gần đó. NHEJ có thể đưa các phần chèn hoặc xóa ngẫu nhiên (indels) vào các vị trí phân cắt, dẫn đến tạo ra các đột biến dịch khung hoặc các codon dừng sớm trong khung đọc mở (ORF) của gen mục tiêu, cuối cùng làm bất hoạt các gen mục tiêu.
Ngoài ra, HDR có thể đưa ra các sửa đổi bộ gen chính xác tại vị trí mục tiêu bằng cách sử dụng các khuôn mẫu sửa chữa DNA tương đồng. Hơn nữa, việc xóa đoạn lớn và loại bỏ đồng thời nhiều gen có thể đạt được bằng cách sử dụng nhiều sgRNA nhắm mục tiêu vào một gen hoặc nhiều gen. Chính vì vậy công cụ CRISPR được ví như một chiếc “kéo di truyền” giúp các nhà khoa học có thể dùng làm “phẫu thuật phân tử” nhờ khả năng cắt một cách chính xác tại vị trí mong muốn và từ đó giúp chỉnh sửa hệ gen trong tế bào.
Một số ứng dụng tiêu biểu của công nghệ CRISPR/Cas9 trong các bệnh di truyền đơn gene
Bệnh di truyền đơn gen (Monogenic diseases) đề cập đến các bệnh di truyền gây ra bởi đột biến của một alen đơn hoặc một cặp alen trên một cặp nhiễm sắc thể tương đồng. Có hơn 6600 bệnh đơn gen được biết đến trên toàn thế giới, bệnh β-thalassemia, bệnh hồng cầu hình liềm (SCD), bệnh máu khó đông B (HB), viêm võng mạc sắc tố (RP), bệnh teo bẩm sinh leber loại 10 (LCA10), bệnh loạn dưỡng cơ duchenne (DMD) , hội chứng progeria Hutchinson-gilford (HGPS), bệnh tyrosin máu di truyền (HT), bệnh xơ nang (CF), v.v.. Hầu hết các bệnh đơn gen đều là các bệnh hiếm gặp, chưa có phương pháp điều trị hiệu. Ngày nay, nhiều mô hình động vật mắc bệnh đơn gen đã được điều trị bằng liệu pháp gen qua công nghệ CRISPR. Hơn nữa, thậm chí đã có một số thử nghiệm lâm sàng CRISPR đối với các bệnh đơn gen đang được thực hiện.
Bệnh β-Thalassaemia
β-Thalassaemia, một bệnh thiếu máu tán huyết di truyền, là một trong những bệnh đơn gen phổ biến và đe dọa sức khỏe nhất trên thế giới. Nó được đặc trưng bởi đột biến gen β-globin (HBB), dẫn đến thiếu máu nghiêm trọng do giảm mức hemoglobin (Hb). Hiện tại, cách duy nhất để chữa bệnh β-thalassemia là ghép tế bào gốc tạo máu (HSCT). Tuy nhiên, chi phí điều trị cao và thiếu người hiến tặng đã hạn chế ứng dụng lâm sàng của phương pháp này. Các liệu pháp khác như truyền máu chỉ có thể duy trì sự sống cho bệnh nhân chứ không thể chữa khỏi bệnh. Để điều trị tốt hơn bệnh β-thalassemia, các nhà nghiên cứu đã chuyển sự chú ý sang liệu pháp gen. Một ý tưởng kỹ thuật chính là sửa chữa gen β-globin khiếm khuyết của iPSC ở bệnh nhân mắc bệnh β-thalassemia bằng công nghệ CRISPR/Cas9, sau đó hồng cầu có thể được sản xuất bình thường và bệnh có thể được chữa khỏi.
Bệnh hồng cầu hình liềm (Sickle cell anemia-SCD)
Ngoài ra, hệ thống CRISPR/Cas cũng đã được sử dụng để điều trị các bệnh về huyết học khác, chẳng hạn như bệnh hồng cầu hình liềm (SCD) và bệnh máu khó đông B (HB). SCD là một bệnh đơn gen gây ra bởi đột biến nucleotide đơn trong gen β-globin ở người, dẫn đến sự thay thế acid glutamic bằng valine và tạo ra một bản sao bất thường của β-globin, được gọi là hemoglobin S (HbS). Hệ thống CRISPR/Cas9 đã được sử dụng để điều trị SCD bằng cách sửa chữa đột biến gen β-globin hoặc kích hoạt lại biểu hiện HbF . HB là một bệnh rối loạn chảy máu di truyền liên kết với nhiễm sắc thể X do thiếu yếu tố đông máu IX và phương pháp điều trị phổ biến nhất đối với bệnh Hemophilia B là bổ sung yếu tố đông máu. Huai và cộng sự đã tiêm plasmid Cas9-sgRNA trần và DNA của người hiến vào chuột trưởng thành của mô hình chuột HB đột biến F9 để chỉnh sửa gen. Trong khi đó, Cas9/sgRNA cũng được tiêm vi mô vào tế bào mầm của mẫu chuột HB này để chỉnh sửa gen. Cả thí nghiệm in vivo và ex vivo đều đủ để khắc phục tình trạng thiếu đông máu. Guan và cộng sự đã sửa chữa đột biến F9 Y371D ở chuột HB bằng cách sử dụng chỉnh sửa bộ gen tại chỗ qua trung gian CRISPR/Cas9, giúp cải thiện đáng kể hiệu quả cầm máu và tăng khả năng sống sót của chuột HB.
Hội chứng Progeria Hutchinson-Gilford (HGPS)
Hội chứng HGPS là một rối loạn di truyền gây chết người hiếm gặp với đặc điểm lão hóa nhanh. Một đột biến điểm trong exon 11 của gen lamin A sẽ kích hoạt các vị trí cryptic splice, dẫn đến việc tạo ra một lamin A bị cắt cụt gọi là progerin. Tuy nhiên, liệu pháp gen dựa trên CRISPR/Cas đã mở ra triển vọng rộng lớn trong điều trị HGPS. Việc sử dụng các thành phần CRISPR/Cas9 do AAV phân phối vào chuột HGPS có thể làm giảm biểu hiện của progerin, từ đó cải thiện tình trạng sức khỏe và kéo dài tuổi thọ của chuột HGPS.
Một số ứng dụng tiêu biểu của công nghệ CRISPR/Cas9 trong các bệnh truyền nhiễm
Trong những năm gần đây, liệu pháp gen dần được áp dụng để điều trị các bệnh truyền nhiễm do virus. Biến đổi tế bào vật chủ để tránh nhiễm virus hoặc ngăn chặn sự tăng sinh, phát triển và lây truyền của virus là hai chiến lược chính trong liệu pháp gen đối với các bệnh truyền nhiễm do virus.
CRISPR/Cas9 trong việc điều trị nhiễm HIV
Virus gây suy giảm miễn dịch ở người (HIV), một loại retrovirus, chủ yếu tấn công hệ thống miễn dịch của con người, đặc biệt là tế bào T-CD4+. Khi tế bào người bị HIV xâm chiếm, các chuỗi virus có thể được tích hợp vào bộ gen của vật chủ, ngăn chặn khả năng miễn dịch tế bào và thể dịch đồng thời gây ra hội chứng suy giảm miễn dịch mắc phải (AIDS). Hiện vẫn chưa có phương pháp chữa khỏi bệnh AIDS nhưng nó có thể được điều trị. Mặc dù liệu pháp kháng virus có thể ức chế sự sao chép của HIV-1, nhưng các trình tự virus vẫn tồn tại trong bộ gen của vật chủ và chúng có thể được kích hoạt lại bất kỳ lúc nào. Hệ thống CRISPR/Cas9 có thể nhắm đến vùng long-term repeat của HIV-1 (LTR) và tiêu diệt các tiền virus HIV-1. Do đó có thể loại bỏ hoàn toàn HIV-1 khỏi bộ gen của các tế bào chủ bị nhiễm bệnh. Ngoài ra, khả năng kháng lại nhiễm HIV-1 có thể được tạo ra bằng cách loại bỏ gen CCR5 đồng thụ thể HIV trong tế bào T-CD4+.
CRISPR/Cas9 trong việc điều trị nhiễm HPV
Ung thư cổ tử cung là khối u ác tính phụ khoa phổ biến thứ hai. Tỷ lệ mắc bệnh ngày càng tăng qua từng năm và đặc biệt là những người trẻ tuổi dễ mắc bệnh này. Người ta phát hiện ra rằng sự xuất hiện của ung thư cổ tử cung có liên quan chặt chẽ đến nhiễm trùng HPV (papillomavirus ở người). HPV là một loại virus DNA vòng kép, các gen E6 và E7 nằm ở vùng đầu của HPV16 là các gen gây ung thư. Các nhà nghiên cứu đã thiết kế các sgRNA nhắm mục tiêu vào các gen E6 và E7 để ngăn chặn sự biểu hiện của protein E6 và E7, sau đó sự biểu hiện của p53 và pRb được khôi phục lại bình thường, cuối cùng làm tăng quá trình apotosis (chu trình chết của tế bào) và ức chế sự phát triển của khối u dưới da trong các thí nghiệm in vivo. Hơn nữa, sự phát triển của vi rút HPV đã bị ngăn chặn thông qua việc cắt bỏ gen E6/E7 và virus trong cơ thể có thể bị loại bỏ.
Tài liệu tham khảo
Tìm hiểu về hệ thống chỉnh sửa hệ gen CRISPR. (n.d.). Vinmec.com. Retrieved April 9, 2024, from https://www.vinmec.com/vi/tin-tuc/thong-tin-suc-khoe/suc-khoe-tong-quat/tim-hieu-ve-he-thong-chinh-sua-he-gen-crispr/
Ceccaldi R., Rondinelli B., D’Andrea A.D. Repair pathway choices and consequences at the double-strand break. Trends Cell Biol. 2016;26:52–64.
Chen H., Choi J., Bailey S. Cut site selection by the two nuclease domains of the Cas9 RNA-guided endonuclease. J Biol Chem. 2014;289:13284–13294.
Cong L., Ran F.A., Cox D., Lin S., Barretto R. Multiplex genome engineering using CRISPR/Cas systems. Science. 2013;339:819–823.
Deltcheva E., Chylinski K., Sharma C.M., Gonzales K., Chao Y. CRISPR RNA maturation by trans-encoded small RNA and host factor RNase III. Nature. 2011;471:602–607.
Deveau H., Garneau J.E., Moineau S. CRISPR/Cas system and its role in phage-bacteria interactions. Annu Rev Microbiol. 2010;64:475–493.
Horvath P., Barrangou R. CRISPR/Cas, the immune system of bacteria and archaea. Science. 2010;327:167–170.
Introduction to the CRISPR/Cas9 system. (n.d.). Takarabio.com. Retrieved April 9, 2024, from https://www.takarabio.com/learning-centers/gene-function/gene-editing/gene-editing-tools-and-information/introduction-to-the-crispr/cas9-system
Jiang F., Doudna J.A. CRISPR-Cas9 structures and mechanisms. Annu Rev Biophys. 2017;46:505–529.
Jinek M., Chylinski K., Fonfara I., Hauer M., Doudna J.A. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science. 2012;337:816–821.
Koonin E.V., Makarova K.S. CRISPR-Cas: an adaptive immunity system in prokaryotes. F1000 Biol Rep. 2009;1:95
Koonin E.V., Makarova K.S., Zhang F. Diversity, classification and evolution of CRISPR-Cas systems. Curr Opin Microbiol. 2017;37:67–78.
Lieber M.R. The mechanism of double-strand DNA break repair by the nonhomologous DNA end-joining pathway. Annu Rev Biochem. 2010;79:181–211.
Makarova K.S., Haft D.H., Barrangou R., Brouns S.J., Charpentier E. Evolution and classification of the CRISPR-Cas systems. Nat Rev Microbiol. 2011;9:467–477.
Mali P., Yang L., Esvelt K.M., Aach J., Guell M. RNA-guided human genome engineering via Cas9. Science. 2013;339:823–826.
Minkenberg B., Wheatley M., Yang Y. CRISPR/Cas9-enabled multiplex genome editing and its application. Prog Mol Biol Transl Sci. 2017;149:111–132.
Patsali P., Kleanthous M., Lederer C.W. Disruptive technology: CRISPR/Cas-based tools and approaches. Mol Diagn Ther. 2019;23:187–200.
Ran F.A., Hsu P.D., Wright J., Agarwala V., Scott D.A. Genome engineering using the CRISPR-Cas9 system. Nat Protoc. 2013;8:2281–2308.
Richardson C.D., Ray G.J., DeWitt M.A., Curie G.L., Corn J.E. Enhancing homology-directed genome editing by catalytically active and inactive CRISPR-Cas9 using asymmetric donor DNA. Nat Biotechnol. 2016;34:339–344.
San Filippo J., Sung P., Klein H. Mechanism of eukaryotic homologous recombination. Annu Rev Biochem. 2008;77:229–257.
Weterings E., Chen D.J. The endless tale of non-homologous end-joining. Cell Res. 2008;18:114–124.
Xu, Y., & Li, Z. (2020). CRISPR-Cas systems: Overview, innovations and applications in human disease research and gene therapy. Computational and Structural Biotechnology Journal, 18, 2401-2415.
You, L., Tong, R., Li, M., Liu, Y., Xue, J., & Lu, Y. (2019). Advancements and obstacles of CRISPR-Cas9 technology in translational research. Molecular Therapy-Methods & Clinical Development, 13, 359-370.
Zhang, H., Qin, C., An, C., Zheng, X., Wen, S., Chen, W., … & Wu, Y. (2021). Application of the CRISPR/Cas9-based gene editing technique in basic research, diagnosis, and therapy of cancer. Molecular Cancer, 20, 1-22.





