Phương pháp tổng hợp mới đã được phát triển để giúp oligonucleotide có vùng Abasic site ổn định tại bất kỳ vị trí nào trong chuỗi khi sử dụng tetrahydrofuran biến đổi, có cấu trúc giống với 2′-deoxyribofuranose, như một phân tử tương đồng với cấu trúc abasic site.
Khi diễn ra quá trình thủy phân các nhóm nucleotide trong DNA có thể dẫn đến tình trạng nucleotide bị khử base nitơ và hình thành các vùng abasic site (vị trí trong DNA không có gốc purine hoặc pyrimidine). Cụ thể, thông thường tại các vị trí dA (nu A và nu G) sẽ dễ bị thủy phân và gây ra hiện tượng tách khử purine (depurination), hình thành vùng abasic site. Mặc dù quá trình này diễn ra chậm, nhưng khi ở điều kiện môi trường acid (pH thấp), phản ứng sẽ xảy ra nhanh hơn và đặc biệt là khi các bazơ đã bị oxy hóa. Các base bị tổn thương này cũng có thể bị loại bỏ bởi enzyme thông qua hoạt động của DNA N-glycosylases (Base Excision Repair).
Abasic residue (dR) tồn tại chủ yếu dưới dạng chu kỳ và cấu trúc của nó được hiển thị trong Hình 1. Trạng thái vùng abasic site thường thể hiện tính ổn định kém, đặc biệt là ở môi trường bazơ. Điều này là do tính không ổn định của cấu trúc aldehyde, tautomeric của chu kỳ đối với quá trình ß-elimination. Phản ứng phân hủy này dẫn đến phân cắt chuỗi (chain scission) tại vùng abasic site với sự hình thành vùng 5’ phosphate biến đổi (5′-phosphate segment) và vùng 3′ biến đổi (3′-modified segment).
Do tính không ổn định của vùng abasic residue, việc tạo ra biến thể này thông qua phương pháp tổng hợp hóa học trở nên khó thực hiện. Tuy nhiên, một số bài báo thu nhận kết quả tốt khi sử dụng tetrahydrofuran biến đổi như dSpacer tetrahydrofuran analogue giúp ổn định phản ứng. Biến thể (Hình 1) thiếu gốc 1′-OH của dR mang tính ổn định trong quá trình tổng hợp, tinh sạch oligo và lưu trữ. Chúng có khả năng tổng hợp vùng abasic residue bằng cách sử dụng N-uracil glycosylase để loại bỏ uracil từ 2′-deoxyuridine residue.
Trong phương pháp hóa học từ Rayner, abasic site được bảo vệ bằng một nhóm photolabile 2-nitrobenzyl (Hình 1) trong suốt quá trình tổng hợp và tinh sạch oligo. Nhóm 2-nitrobenzyl sau đó được loại bỏ thông qua phản ứng quang phân (photolysis) để tạo ra abasic site. Tuy nhiên, cần lưu ý về việc hình thành thymine dimer trong quá trình này. Một số phương pháp khác đã được sử dụng để tổng hợp vùng abasic site, nhưng cho đến nay, quá trình tổng hợp monomer vẫn còn đang được nghiên cứu.
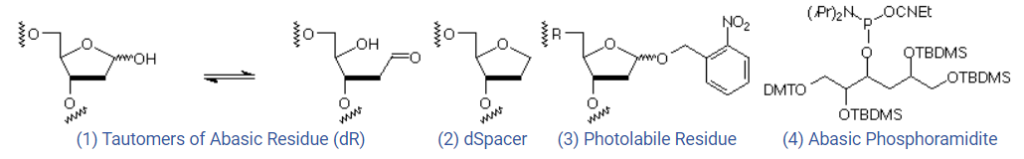
(Nguồn: Glen Research)
1. Tổng hợp Oligonucleotide vùng abasic site
Một phương pháp hóa học được nhắc đến khi tổng hợp các oligonucleotide mạch đơn và đôi có chứa vùng abasic site bằng điều kiện không quá gắt gao và khả năng cho ra các phản ứng phụ rất thấp. Trong quá trình này, hợp chất 3-deoxyhexitol được dùng như một monomer (Hình 1), được bảo vệ để ngăn chặn phản ứng không mong muốn.
Sau khi tổng hợp oligo theo điều kiện tiêu chuẩn, các nhóm bảo vệ silyl của vùng (hình 2) được loại bỏ bằng axit nước. (Điều này có thể thực hiện cùng với quá trình loại bỏ trityl trong bước cuối cùng của quá trình tinh sạch bằng DMT-ON.) Chúng tạo ra một dạng diol (hình 2), sau đó được xử lý với sodium periodate để tạo thành aldehyde và formaldehyde. Aldehyde này sau đó ngay lập tức xoắn thành một cấu trúc mới – đường abasic cyclic sugar (dR).
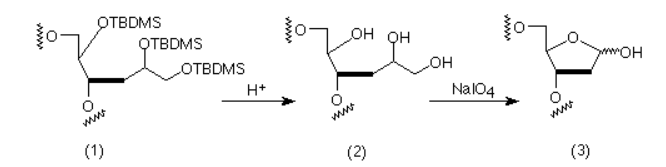
2. Tính ổn định của oligonucleotide
Với sự xuất hiện của oligonucleotide chứa vùng abasic site, được chứng minh là ổn định trong dung dịch đệm axetat triethylammonium buffer 0.2M (pH6) ở 5°C hoặc thấp hơn. Tuy nhiên, trạng thái này ít ổn định ở 55°C (khoảng 7 giờ) và kém hơn khi ở nhiệt độ phòng (khoảng 30 ngày). Đáng chú ý, abasic site bị phân hủy hoàn toàn trong quá trình bay hơi cho đến khi đông khô.
3. Đặc điểm cấu trúc Oligonucleotide
Đối với đặc điểm cấu trúc, các nghiên cứu về tính nóng chảy của oligo chứa abasic site đã được tiến hành. Kết quả cho thấy rằng abasic site không tạo thành cặp ổn định với bất kỳ trong 4 base nào (adenine, thymine, cytosine, và guanine) trên chuỗi bổ sung, tương tự với dSpacer. Nghiên cứu cũng đánh giá các đặc điểm vật lý khác và mối liên quan của chúng đối với tổn thương và sửa chữa DNA.
Pannel ứng dụng trong chẩn đoán Thalassemia
Tổng quan Thalassemia Giới thiệu Thalassemia Thalassemia (hay còn được gọi với tên bệnh tan máu bẩm sinh) là một bệnh lý huyết học di truyền có tỷ lệ lưu hành cao trên toàn cầu và là một vấn đề…
Ảnh hưởng của TaqMan probe đến độ đặc hiệu và độ nhạy trong Realtime PCR
TaqMan Probe đóng vai trò trung tâm trong việc đảm bảo độ chính xác, độ đặc hiệu và độ nhạy của phản ứng trong kỹ thuật Real-time PCR
TAQMAN PROBE VÀ CÁC TIÊU CHÍ QUAN TRỌNG KHI THIẾT KẾ PROBE TRONG REAL TIME PCR
Probe (đầu dò) trong sinh học phân tử là một đoạn oligonucleotide (DNA hoặc RNA sợi đơn) ngắn, được đánh dấu bằng các phân tử phát tín hiệu (thường là các chất phát huỳnh quang). Probe được thiết kế để…
HPLC Là Gì? Ứng Dụng Của HPLC Trong Tinh Sạch và Phân Tích Oligonucleotide
HPLC (High Performance Liquid Chromatography) – Sắc ký lỏng hiệu năng cao là một kỹ thuật phân tích được sử dụng để tách, định tính hoặc định lượng các chất, thành phần trong một hỗn hợp chất lỏng.
CÁC PHƯƠNG PHÁP TINH SẠCH OLIGONUCLEOTIDE
Oligonucleotide là những phân tử DNA hoặc RNA mạch đơn hoặc mạch đôi có kích thước ngắn thường được sử dụng trong các ứng dụng sinh học phân tử, y học và nghiên cứu khoa học. Các trình tự oligonucleotide…
Dịch vụ OligoX
Tổng hợp Oligonucleotide bao gồm các sản phẩm PCR, qPCR Primer, Primer/Probe biến đổi, Trình tự RNA, Amplicon và các tổng hợp đặc biệt
Nguồn tham khảo
- Glen Research. https://www.glenresearch.com/reports/gr14-13
- M. Takeshita, C.N. Chang, F. Johnson, S. Will, and A.P. Grollman, J. Biol. Chem., 1987, 262, 10171-10179. https://pubmed.ncbi.nlm.nih.gov/2440861/
- M.W. Kalnik, C.N. Chang, A.P. Grollman, and D.J. Patel, Biochemistry, 1988, 27, 924-931.
- D. Péoc’h, A. Meyer, J.-L. Imbach, and B. Rayner, Tetrahedron Lett., 1991, 32, 207.
- A. Laayoun, J.L. Decout, E. Defrancq, and J. Lhomme, Tetrahedron Lett., 1994, 35, 4991-4994.
- R.S. Coleman and R.M. Pires, Nucleosides and Nucleotides, 1999, 18, 2141-2146.
- J.T. Hwang, K.A. Tallman, and M.M. Greenberg, Nucleic Acids Res., 1999, 27, 3805-10.
- M. Jourdan, J. Garcia, E. Defrancq, M. Kotera, and J. Lhomme, Biochemistry, 1999, 38, 3985-95.
- I.G. Shishkina and F. Johnson, Chem Res Toxicol, 2000, 13, 907-912.
- J. Lhomme, J.F. Constant, and M. Demeunynck, Biopolymers, 1999, 52, 65-83.