1. Tổng quan về HPLC
HPLC (High Performance Liquid Chromatography) – Sắc ký lỏng hiệu năng cao. Đây là một kỹ thuật phân tích được sử dụng để tách, định tính hoặc định lượng các chất, thành phần trong một hỗn hợp chất lỏng.
2. Lịch sử của HPLC
Bản chất của phương pháp HPLC là phương pháp sắc ký cổ điển nhưng được phân tách dưới điều kiện áp suất cao với sự hỗ trợ của các các máy bơm cao áp. Nguồn gốc của từ viết tắt HPLC, được giới thiệu lần đầu tiên bởi Giáo sư Csaba Horváth trong bài báo Pittcon năm 1970, áp suất cao lúc này được sử dụng để tạo ra dòng chảy qua cột sắc ký. Lúc này các máy bơm chỉ có khả năng tạo ra áp suất 500 psi tương đương với 35 bar. Ở thời điểm này được gọi là sắc ký lỏng áp suất cao (high pressure liquid chromatography) . Đầu những năm 1970 chứng kiến bước nhảy vọt về công nghệ, các thiết bị HPLC mới được phát triển có áp suất lên tới 6.000 psi (400 bar) và kết hợp các kim tiêm mẫu, đầu dò và cột được cải tiến. . Với những tiến bộ liên tục về hiệu suất trong thời gian này bao gồm: các hạt nhỏ hơn, áp suất cao hơn dẫn đến tên của kỹ thuật này đã đổi thành sắc ký lỏng hiệu năng cao (high performance liquid chromatography) nhưng từ viết tắt HPLC vẫn giữ nguyên.
3. Cấu tạo HPLC
Một hệ thống HPLC thường bao gồm nhiều bộ phận khác nhau, trong đó các bộ phận chính thường bao gồm:
- Bình chứa pha động (Solvent Reservoir): một máy HPLC thông thường có từ 2 đến 4 bình chứa pha động để trộn các dung môi khác nhau để phân tách và rửa giải theo tỷ lệ mong muốn.
- Bộ khử khí (Degasser): có chức năng hỗ trợ loại bỏ những bọt khí còn sót lại trong dung môi pha động để giúp bộ phận bơm hoạt động ổn định và chính xác, do khi bọt khí quá nhiều không thể loại trừ hết chúng thì bộ phận bơm cao áp có thể không hút được dung môi, ảnh hưởng tới tỷ lệ phối trộn giữa các dung môi và từ đó dẫn đến sai lệch kết quả phân tích cuối cùng của hệ thống.
- Bơm cao áp (High-Pressure Pump): có chức năng bơm pha động đi qua hệ thống với áp suất cao để thực hiện quá trình phân tách sắc ký, thường đạt áp suất khoảng 1000–5000 psi tùy thuộc vào tốc độ dòng sử dụng.
- Bộ tiêm mẫu (Injector hoặc Autosa mpler): có chức năng tiêm mẫu cần phân tích vào cột phân tích.
- Cột sắc ký (Column): Là nơi diễn ra quá trình phân tách sắc ký và thường được giữ ở nhiệt độ ổn định trong buồng điều nhiệt cột. Cột sắc ký được làm từ thép không gỉ với chiều dài khoảng 50 – 300 mm với đường kính trong từ 2 – 5 mm và thường được nhồi bằng các hạt silica nhỏ có kích thước từ 2.5 – 5 µm được biến đổi để phù hợp với loại phương pháp HPLC (pha đảo, pha thường, trao đổi ion)
- Đầu dò (Detector): có chức năng phát hiện và ghi nhận tín hiệu của các hợp chất khi chúng ra khỏi cột sắc ký để định tính và định lượng. Tùy thuộc vào tính chất của chất phân tích mà người ta chọn loại đầu dò phù hợp. Các loại đầu dò phổ biến thường được sử dụng bao gồm: UV-VIS, PDA, RI, EC, FL.
- Bộ xử lý dữ liệu (Data System/Software): có chức năng thu thập và xử lý tín hiệu từ đầu dò, tạo sắc ký đồ (chromatogram) để phân tích, ghi nhận thời gian lưu (retention time). ,đo diện tích hoặc chiều cao các đỉnh (peaks) để định lượng.

4. Nguyên lý hoạt động của HPLC
Quá trình hoạt động, phân tách hỗn hợp chất của HPLC thường dựa trên sự tương tác, sự khác biệt về ái lực của hỗn hợp chất cần phân tách với pha động trong dung môi và pha tĩnh trong cột sắc ký. Khi hỗn hợp mẫu được tiêm vào hệ thống, hỗn hợp chất cần phân tách sẽ di chuyển qua cột với tốc độ khác nhau tùy theo mức độ tương tác, ái lực của mỗi chất với pha tĩnh và pha động. Các chất, phân tử có ái lực mạnh với pha tĩnh sẽ liên kết mạnh với cột và di chuyển chậm hơn. Còn các phân tử có ái lực mạnh với pha động sẽ bị kéo theo dòng dung môi và di chuyển nhanh hơn từ đó ra khỏi cột nhanh hơn như hình dưới đây.

Tùy thuộc vào bản chất của mẫu cần phân tích, bản chất của pha tĩnh và cơ chế phân tách được sử dụng, có thể chia HPLC thành các loại như sau:
- HPLC pha thuận (Normal-Phase HPLC): Sử dụng các pha tĩnh phân cực và pha động không phân cực. Phương pháp này phù hợp để tách các hợp chất không phân cực.
- HPLC pha đảo (Reverse-Phase HPLC): Sử dụng pha tĩnh không phân cực và pha động phân cực. Đây là loại sắc ký lỏng hiệu suất cao được sử dụng rộng rãi và phổ biến nhất cho các hợp chất phân cực, phù hợp với nhiều ứng dụng chẳng hạn như trong phân tích dược phẩm và tách sinh hóa
- Sắc ký loại trừ kích thước (Size Exclusion Chromatography): các phân tử, các chất được phân tách dựa trên kích thước, với các phân tử có kích thước lớn hơn di chuyển nhanh hơn và rửa giải ra trước. Nó đặc biệt hữu ích để phân tích polyme và protein.
- Sắc ký trao đổi ion (Ion-Exchange Chromatography): quá trình phân tách của phương pháp này dựa trên sự trao đổi, tương tác điện tích giữa chất cần phân tích và pha tĩnh. Trong đó pha tĩnh thường mang nhóm mang điện tích trái dấu với nhóm điện tích của chất cần phân tách.
- Sắc ký ái lực (Affinity Chromatograph): kỹ thuật có tính đặc hiệu cao này sử dụng các tác nhân có liên quan về mặt sinh học (ví dụ: kháng thể) làm pha tĩnh để tách các phân tử sinh học.
5. Ứng dụng của HPLC trong oligonucleotide
Ứng dụng của HPLC trong các oligonucleotide nói riêng và các sản phẩm sinh học nói chung đã được chứng minh là hữu ích. Trong đó, tinh sạch các sản phẩm oligonucleotide và phân tích độ tinh sạch oligonucleotide là 2 ứng dụng phổ biến nhất. Do bản chất của oligonucleotide là những phân tử phân cực (ưa nước) và mang điện tích âm ở pH 7, nên phương pháp thường được sử dụng để tinh sạch oligonucleotide hiện nay là Ion pair reverse-phase HPLC) và Ion-exchange HPLC. Quá trình chọn phương pháp tinh sạch oligo bằng HPLC phù hợp sẽ tùy thuộc vào chiều dài và đặc tính của oligo cần tinh sạch.
5.1. HPLC pha đảo ghép cặp ion (Ion pair reverse-phase HPLC)
Sắc ký lỏng hiệu năng cao pha đảo ghép cặp ion (IP-RP-HPLC) có bản chất là kỹ thuật HPLC pha đảo nhưng được kết hợp bổ sung thêm các thuốc thử ghép cặp ion trong pha động để tăng cường khả năng phân tách các hợp chất ion và phân cực từ đó giúp tăng độ phân giải, độ tinh sạch của sản phẩm. Các tác nhân ghép cặp ion thường có cấu trúc chung gồm: một nhóm kỵ nước bám vào pha tĩnh và một nhóm tích điện âm hoặc dương tùy thuộc vào loại tác nhân ghép cặp ion sử dụng. Do bản chất của các oligo là các phân tử mang điện tích âm, nên các chất ghép cặp ion thường mang điện tích dương có thể sử dụng như là TEA, DIEA, DMCHA như hình bên dưới đây.

Cơ chế phân tách của IP-RP-HPLC là dựa trên tính kỵ nước và chiều dài của phân tử oligonucleotide cần tinh sạch. Những phân tử oligonucleotide mang điện tích âm lúc này sẽ liên kết với các chất ghép cặp ion được bổ sung trong pha động và những chất ghép cặp ion một đầu còn lại này sẽ liên kết với pha tĩnh (Cột sắc ký C18 hoặc C8). Những phân tử oligo có tính kỵ nước và có kích thước dài có xu hướng được giữ lại lâu hơn, do oligonucleotide dài hơn, mang nhiều nhóm phosphate (điện tích âm) hơn, và tính kỵ nước của oligo sẽ liên kết mạnh hơn với pha tĩnh thông qua tương tác kỵ nước như bản chất của kỹ thuật này như hình bên dưới đây.

Hiện nay, đây là phương pháp tinh sạch hiệu quả đối với các oligonucleotide biến đổi có gắn huỳnh quang (như taqman probe) vì những phân tử huỳnh quang có tính kỵ nước, từ đó tạo sự khác biệt giữa trình tự mục tiêu và trình tự lỗi, làm cơ sở giúp phân tách hiệu quả trình tự mục tiêu khỏi các trình tự lỗi có kích thước ngắn và các trình tự lỗi không gắn huỳnh quang. Hơn nữa, đây là phương pháp được lựa chọn để tổng hợp quy mô lớn do khả năng tự động hóa của hệ thống. Tuy nhiên, khả năng phân tách dựa trên tính kỵ nước có thể bị ảnh hưởng theo chiều dài của oligonucleotide. Do đó, kỹ thuật này thường không được khuyến nghị để tinh chế oligonucleotide >60 bases. Mặc dù có thể tinh chế oligonucleotide dài hơn (lên đến 80 bases, trong một số trường hợp dài hơn) bằng phương pháp này, nhưng độ tinh khiết và năng suất có thể bị ảnh hưởng. Các sản phẩm oligo sau khi tinh sạch bằng IP-RP-HPLC thường có độ tinh khiết >90% (thông qua phân tích HPLC).
5.2. Sắc ký lỏng hiệu năng trao đổi ion (IE-HPLC)
Sắc ký lỏng hiệu năng cao trao đổi ion (IE-HPLC) (cụ thể là trao đổi anion) dựa trên số lượng nhóm tích điện âm của nhóm phosphate trong khung xương chính của oligonucleotide. Phương pháp trao đổi anion liên quan đến việc sử dụng các pha động có nồng độ muối cao như Nacl trên các cột có chứa các pha tĩnh amoni. Các trình tự lỗi có kích thước ngắn (shortmer) thường có số lượng điện tích âm ít hơn so với trình tự mục tiêu do đó các trình tự lỗi thường có liên kết yếu với cột nên được rửa giải sớm hơn so với trình tự mục tiêu . Tuy nhiên, IE-HPLC bị giới hạn bởi độ dài, thường khoảng 40 bases. Các oligonucleotide dài hơn dẫn đến khả năng phân tách thấp hơn giữa trình tự mục tiêu và trình tự lỗi; và do đó, độ tinh khiết thường thấp hơn và kém nhất quán hơn.

IEX-HPLC và IP-RP-HPLC đều là hai phương pháp tinh sạch oligo hiệu quả, nhưng lựa chọn phương pháp nào phù hợp sẽ tùy thuộc vào loại, đặc tính và chiều dài của oligo.
Bảng 1. So sánh giữa phương pháp IP-RP-HPLC và IE-HPLC
| Tiêu chí | IP-RP-HPLC | IE-HPLC |
| Nguyên lý tách | Dựa trên tương tác kỵ nước và pha tĩnh C18/C8. | Dựa trên tương tác điện tích giữa nhóm phosphate (-PO₄³⁻) của oligo và pha tĩnh mang điện tích dương. |
| Pha tĩnh | Cột C18, C8 kỵ nước. | Cột sắc ký mang điện tích dương |
| Pha động | – Dung môi hữu cơ (acetonitril) + chất ghép ion (TEAA, TBA). | – Dung dịch đệm muối tăng dần (NaCl, KCl) để cạnh tranh với oligo. |
| Cơ chế giữ oligo | – Oligo tự nhiên quá phân cực, không giữ được trên cột C18. – Chất ghép cặp ion giúp oligo tương tác với pha tĩnh. | – Oligo tích điện âm (-PO₄³⁻) gắn vào pha tĩnh tích điện dương (cột trao đổi anion). – Khi tăng nồng độ muối, các ion Cl⁻ cạnh tranh với oligo và đẩy nó ra khỏi cột. |
| Chiều dài khuyến nghị | < 60 bases | < 50 bases |
| Loại oligo phù hợp | Phù hợp với các oligo biến đổi có tính kỵ nước như taqman probe, primer có gắn huỳnh quang | Phù hợp với các oligo dễ tạo các cấu trúc thứ cấp như RNA, các oligo có hàm lượng %GC cao |
6. Quy trình tinh sạch oligonucleotide bằng HPLC
Một quy trình tinh sạch oligo đặc trưng thường có những bước chính như sau bao gồm:
Bước 1: Chuẩn bị mẫu và buffer, dung môi
– Hoàn nguyên các mẫu oligo cần tinh sạch trong nước tinh khiết HPLC hoặc trong buffer HPLC được sử dụng.
– Lọc mẫu qua màng lọc 0.22 µm để loại bỏ các cặn tạp chất có thể làm tắc cột HPLC.
Bước 2: Chuẩn bị dung môi, buffer HPLC tinh sạch oligo
– Lọc các dung môi và buffer sử dụng qua màng lọc 0.22 µm để loại bỏ các tạp chất có thể làm tắc nghẽn cột HPLC
– Đánh sóng siêu âm các dung môi và buffer để loại các bọt khí tránh ảnh hưởng đến kết quả phân tích.
Bước 3: Chuẩn bị cột và cài đặt chương trình hệ thống HPLC
– Cột HPLC trước khi sử dụng để tinh sạch sẽ được tiến hành cân bằng cột trong 15 phút
– Chương trình hệ thống chạy HPLC thông thường sẽ có những thông số cần phải cài đặt bao gồm:
- Nhiệt độ: thông thường nhiệt độ hệ thống sẽ được cài đặt ở mức 60oC để phá vỡ các cấu trúc thứ cấp của oligonucleotide có thể hình thành từ đó giúp quá trình tách hiệu quả hơn
- Tốc độ dòng: 1 – 10ml/phút tùy thuộc vào đặc điểm cột HPLC và hệ thống HPLC đang sử dụng
- Bước sóng phát hiện: 260nm và 280nm đối với các oligo tiêu chuẩn như primer, hoặc 260nm và bước sóng huỳnh quang đối với các oligo biến đổi có gắn huỳnh quang như taqman probe.
- Chương trình Gradient rửa giải: Thay đổi tỷ lệ giữa các buffer, dung môi để tạo sự khác biệt giúp phân tách oligonucleotide mục tiêu với các oligo bị lỗi.
Bước 4: Nạp mẫu và phân tích sơ bộ để xác định thời gian lưu của oligo cần tinh sạch
– Các mẫu oligo sau khi chuẩn bị sẽ được tiêm vào hệ thống và chạy chương trình đã cài đặt trước đó.
– Các oligo trước khi tinh sạch thường sẽ có một số sản phẩm lỗi với các thời gian lưu khác nhau như hình bên dưới đây/ Trong đó, các oligo mục tiêu thường sẽ có chiều cao peak lớn nhất và có xu hướng ra trễ hơn so với các trình tự oligo lỗi. Do đó lúc này sẽ tiến hành cài đặt hệ thống để thu nhận các phân đoạn, các peak ở khoảng thời gian từ 25 – 29 phút.

Bước 5: Loại bỏ dung môi
– Các oligo sau khi thu nhận trực tiếp từ máy HPLC thường chứa các dung môi hữu cơ do quá trình tinh sạch HPLC, lúc này cần tiến hành loại bỏ các dung môi hữu cơ bằng các kỹ thuật như đông khô, hoặc sử dụng speedvac.
Bước 6: Hoàn nguyên oligo và kiểm tra nồng độ oligo
– Các oligo sau khi được đông khô hoặc làm khô bằng speedvac sẽ được tiến hành hoàn nguyên trong dung dịch TE để bảo quản và được mang đi đo nanodrop để xác định nồng độ và hòa tan về nồng độ mong muốn.
Bước 7: Kiểm tra chất lượng, độ tinh khiết của oligo sau khi tinh sạch
– Các sản phẩm oligonucleotide sau khi tinh sạch sẽ được kiểm tra, QC độ tinh khiết một lần nữa bằng HPLC để đảm bảo chất lượng sản phẩm tốt nhất khi đến tay khách hàng.
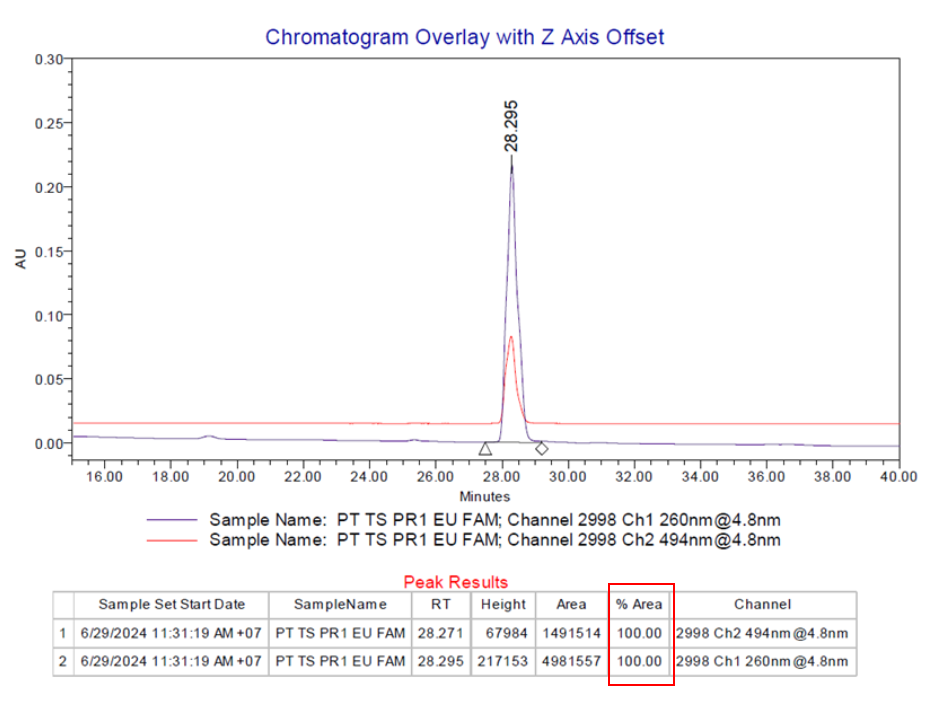
– Các oligo sau khi tinh sạch sẽ được kiểm tra độ tinh khiết ở bước sóng 260 nm và bước sóng 280 hoặc tín hiệu huỳnh quang tùy thuộc vào oligo sản xuất. Độ tinh khiết của sản phẩm thông thường sẽ được xác định dựa trên kết quả sắc ký đồ bằng cách quan sát số lượng peak có trong sắc ký đồ hoặc có thể dựa trên thông số % Area được tính toán trên phần mềm hệ thống của máy HPLC.
– Độ tinh khiết của các sản phẩm Oligo như taqman probe từ OligoX sau khi tinh sạch bằng HPLC luôn cam kết và đảm bảo độ tinh khiết > 90% cho sản phẩm sau khi tinh sạch bằng HPLC như hình bên dưới đây.
7. Tài liệu tham khảo
- HPLC complete guide: All about History, Definition, Principle, Types, Instrumentation, and applications. (2022, March 28). Tech-Publish. https://tech-publish.com/hplc-guide-history-definition-principle-types-instrumentation/
- Science Unfiltered. (2020, June 23). Synthetic oligonucleotides – analysis of their complex structure. SCIENCE UNFILTERED. https://phenomenex.blog/2020/06/23/synthetic-oligonucleotides/
- Vcr V.-T. bị P. (2024, January 11). HPLC là gì? Ứng dụng của HPLC trong kiểm nghiệm thuốc. Vietnamcleanroom – Thiết bị phòng sạch VCR. https://vietnamcleanroom.com/vi/post/hplc-la-gi–ung-dung-cua-hplc-trong-kiem-nghiem-thuoc-1455.htm
- (N.d.-a). Retrieved February 13, 2025, from http://bahttps://www.shimadzu.com/an/service-support/technical-support/analysis-basics/basic/what_is_hplc.html
- (N.d.-b). Sigmaaldrich.com. Retrieved February 13, 2025, from https://www.sigmaaldrich.com/VN/en/technical-documents/technical-article/genomics/dna-and-rna-purification/custom-dna-oligos-purity-verification





