Oligonucleotide là những phân tử DNA hoặc RNA mạch đơn hoặc mạch đôi có kích thước ngắn thường được sử dụng trong các ứng dụng sinh học phân tử, y học và nghiên cứu khoa học. Các trình tự oligonucleotide thường được tạo ra dựa trên phương pháp tổng hợp hóa học, trong đó các đơn phân được sử dụng trong phương pháp hóa học để cấu thành một trình tự oligo, được gọi là phosphoramidite.
Tại sao phải tinh sạch oligonucleotide
Do bản chất của quá trình tổng hợp oligonucleotide là các phản ứng hóa học mà thông thường các phản ứng hóa học không bao giờ đạt được hiệu suất phản ứng là 100%, do đó dẫn đến hình một số sản phẩm phụ lỗi bao gồm:
- Các trình tự lỗi, và các trình tự lỗi này thường có kích thước ngắn hơn trình tự oligonucleotide mục tiêu cần tổng hợp, do hiệu suất phản ứng không đạt được hiệu quả 100% cho nên sẽ có một số nucleotide không ghép nối được trong mỗi chu kỳ tổng hợp từ đó dẫn đến hình thành các trình tự có kích thước ngắn hơn.
- Các tạp chất hóa học bao gồm dung môi, các phân tử nhỏ như các muối hữu cơ được tạo thành từ các phản ứng hóa học trong quy trình tổng hợp.
Việc tinh chế giúp:
- Đảm bảo độ chính xác và cải thiện hiệu quả của thí nghiệm trong các ứng dụng cụ thể như PCR, qPCR hay nghiên cứu liệu pháp gene.
- Đảm bảo độ ổn định và khả năng bảo quản của sản phẩm.
- Đáp ứng các yêu cầu, tiêu chuẩn nghiêm ngặt về chất lượng trong các ứng dụng lâm sàng.
Nguồn gốc của các tạp chất và cách lựa chọn phương pháp tinh sạch
Trong quá trình sản xuất, mỗi nucleotide được ghép nối tuần tự với trình tự đang tổng hợp thông qua phản ứng hóa học phosphoramidite. Trong mỗi chu kỳ ghép nối, có một số tỷ lệ phần trăm trình tự oligo không được ghép nối với nucleotide tiếp theo, nên từ đó tạo ra một hỗn hợp bao gồm: các trình tự mục tiêu chính xác (n) và các trình tự bị đột biến có kích thước ngắn hơn (n-1, n-2, v.v.). Ngoài ra, các tạp chất phân tử nhỏ như muối hữu cơ là sản phẩm phụ của quá trình cắt và khử bảo vệ. Việc lựa chọn phương pháp tinh sạch nên cân nhắc dựa trên các yếu tố sau bao gồm: chiều dài oligo, loại oligo và ứng dụng của oligo, chi phí sản xuất và tinh sạch oligo.
Đối với các oligo tiêu chuẩn có kích thước ngắn hơn nhỏ hơn < 35 bases và được ứng dụng trong các kỹ thuật không cần độ chính xác cao như PCR hoặc RT-PCR thì có thể sử dụng khử muối hoặc catridge để tinh sạch. Còn đối với oligo biến đổi như taqman probe hoặc các oligo được ứng dụng trong các nghiên cứu yêu cầu độ chính xác cao như tạo dòng (cloning), antisense hay trong tế bào sống (in vivo) nên sử dụng phương pháp tinh sạch HPLC. Hình 1 cung cấp một số khuyến nghị về cách lựa chọn phương pháp tinh sạch tùy thuộc vào ứng dụng cũng như phương pháp nghiên cứu.
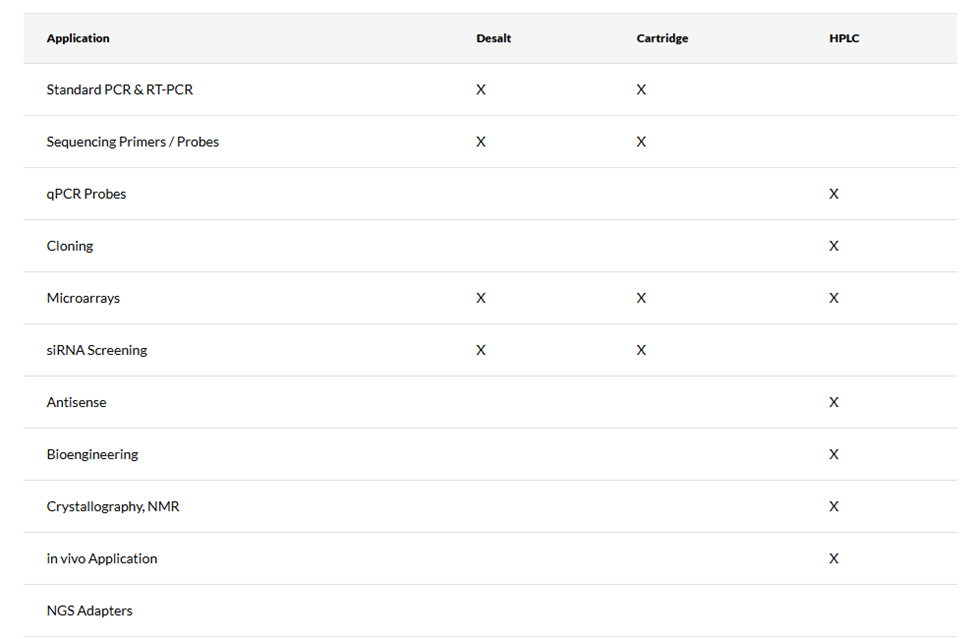
Các phương pháp tinh sạch oligo phổ biến trên thế giới
Phương pháp khử muối
Khử muối là phương pháp tinh sạch cơ bản chỉ loại bỏ được các tạp chất, các phân tử nhỏ như các muối hữu cơ bao gồm: benzamide, acrylonitrile được hình thành do các phản ứng hóa học trong quá trình tổng hợp oligo. Hầu hết các sản p hẩm primer được sử dụng trong kỹ thuật PCR hoặc qPCR thường được tinh sạch bằng khử muối, bởi vì các primer thường có kích thước nhỏ hơn < 35 base, do đó tỷ lệ trình tự lỗi lúc này chỉ chiếm một tỷ lệ ít, đồng thời kỹ thuật PCR không yêu cầu độ chính xác quá nghiêm ngặt khi so sánh với các sản phẩm oligo được sử dụng trên lâm sàng như antisense hoặc gapmer. Do đó các oligo có chiều dài nhỏ hơn < 35 bases có thể sử dụng phương pháp khử muối để tinh sạch. Nhưng đối với các oligo có kích thước > 35 bases nên sử dụng các phương pháp tinh sạch có khả năng loại bỏ được các trình tự lỗi như phương pháp catridge hoặc HPLC.
Hiện tại, kỹ thuật sắc ký lọc gel là một trong những kỹ thuật được sử dụng phổ biến nhất để tinh sạch khử muối cho các trình tự oligo. Nguyên lý của kỹ thuật sắc ký lọc gel là dựa trên sự khác biệt về kích thước của các phân tử cần phân tách. Trong đó, các trình tự oligo cần tinh sạch khử muối sẽ được nạp vào các cột có chứa các lỗ gel. Sau đó những phân tử, tạp chất có kích thước nhỏ sẽ di chuyển xen kẽ qua các lỗ gel nên di chuyển chậm hơn, trong khi đó những phân tử có kích thước lớn như oligo không di chuyển được qua các lỗ gel nên di chuyển nhanh hơn, dẫn đến các trình tự oligo di chuyển ra khỏi cột sớm hơn từ đó phân tách được các tạp chất có kích thước nhỏ như muối.
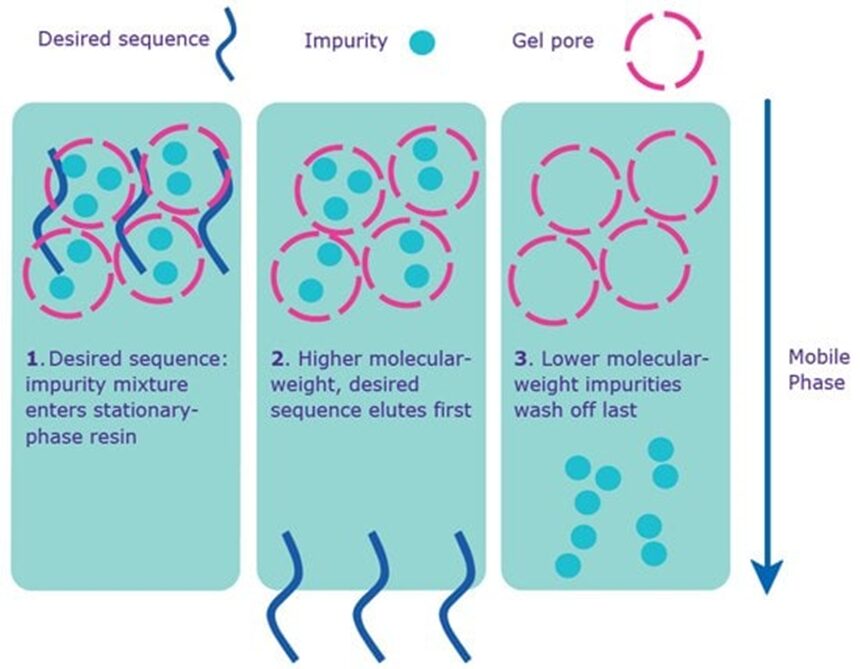
Phương pháp reversed-phase cartridge
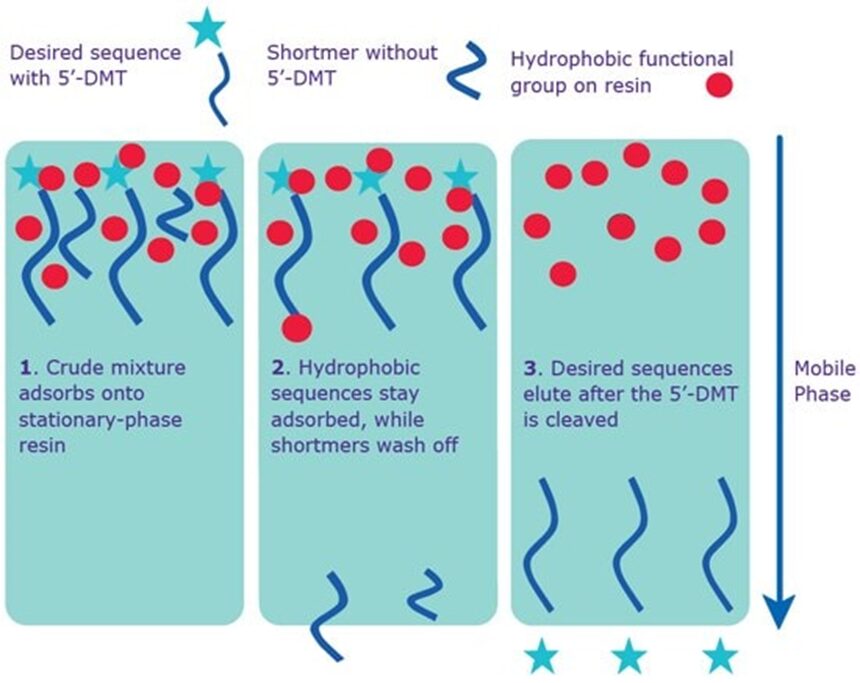
Các trình tự được tinh sạch bằng kỹ thuật catridge pha đảo có độ tinh sạch cao hơn so với phương pháp khử muối, vì kỹ thuật này có khả năng loại bỏ được các trình tự lỗi. Nguyên lý của kỹ thuật này là dựa trên sự khác biệt về tính kỵ nước giữa trình tự mục tiêu có kích thước chính xác (thường được gắn các nhóm 5’-DMT kỵ nước), trong khi đó các trình tự lỗi có kích thước ngắn hơn thường sẽ không được gắn các nhóm 5’-DMT.
Các mẫu oligo cần tinh sạch sẽ được nạp vào cột có chứa các pha tĩnh mang nhóm chức kỵ nước, lúc này các trình tự có kích thước đầy đủ và có chứa nhóm 5’-DMT kỵ nước (Đoạn thẳng có gắn ngôi sao như hình 3) thường có liên kết mạnh với cột nên các trình tự oligo có kích thước chính xác sẽ được giữ lại trên cột, trong khi đó những trình tự lỗi có kích thước ngắn sẽ bị rửa giải sớm hơn. Sau đó sẽ tiến hành loại bỏ nhóm DMT và rồi tiến hành thu nhận trình tự oligo mục tiêu.
Khi chiều dài oligonucleotide tăng lên, tỷ lệ các trình tự lỗi có xu hướng tăng lên và được giữ lại trên cột. Những trình tự lỗi không mong muốn này sẽ không được loại bỏ bằng kỹ thuật catridge và do đó, đối với các oligonucleotide dài hơn > 60 bases, nên sử dụng phương pháp sắc ký lỏng hiệu năng cao (HPLC) hoặc điện di gel polyacrylamide (PAGE).
Sắc ký lỏng hiệu năng cao pha đảo (RP-HPLC)
Sắc ký lỏng hiệu năng cao pha đảo (RP-HPLC) hoạt động theo cùng nguyên lý như kỹ thuật catridge pha đảo. Tuy nhiên, RP-HPLC có khả năng phân tách tốt hơn dẫn đến các sản phẩm có mức độ tinh khiết cao hơn. RP-HPLC là phương pháp tinh sạch hiệu quả đối với các oligonucleotide biến đổi có gắn huỳnh quang vì tính kỵ nước của huỳnh quang giúp phân tách hiệu quả trình tự mục tiêu khỏi các trình tự lỗi có kích thước ngắn và các trình tự lỗi không gắn huỳnh quang. Hơn nữa, RP-HPLC là phương pháp được lựa chọn để tổng hợp quy mô lớn do khả năng tự động hóa của hệ thống.
Tuy nhiên, khả năng phân tách dựa trên tính kỵ nước có thể bị ảnh hưởng theo chiều dài của oligonucleotide. Do đó, RP-HPLC thường không được khuyến nghị để tinh chế oligonucleotide >60 bases. Mặc dù có thể tinh chế oligonucleotide dài hơn (lên đến 80 bases, trong một số trường hợp dài hơn) bằng phương pháp này, nhưng độ tinh khiết và năng suất có thể bị ảnh hưởng xấu. Các sản phẩm oligo sau khi tinh sạch bằng RP-HPLC thường có độ tinh khiết >90% (thông qua phân tích HPLC).
Sắc ký lỏng hiệu suất cao trao đổi ion (IE-HPLC)
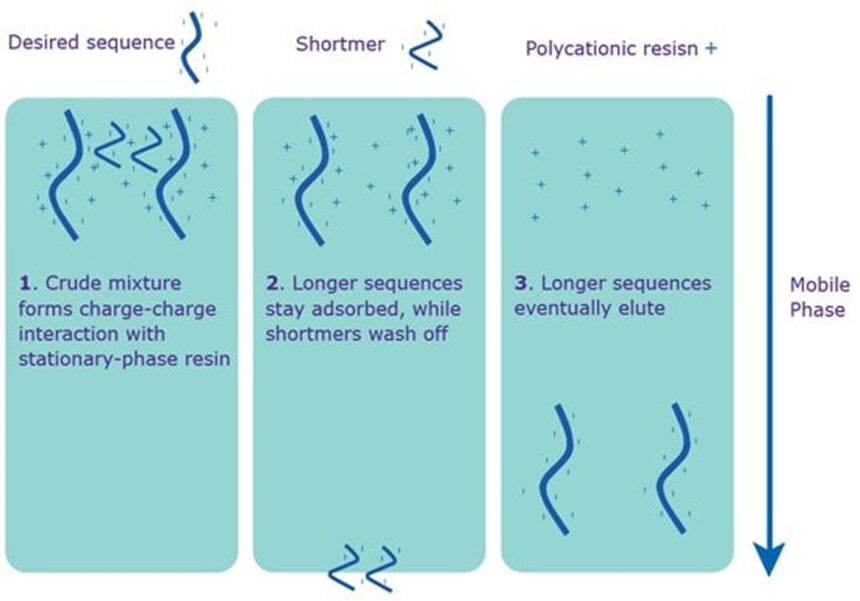
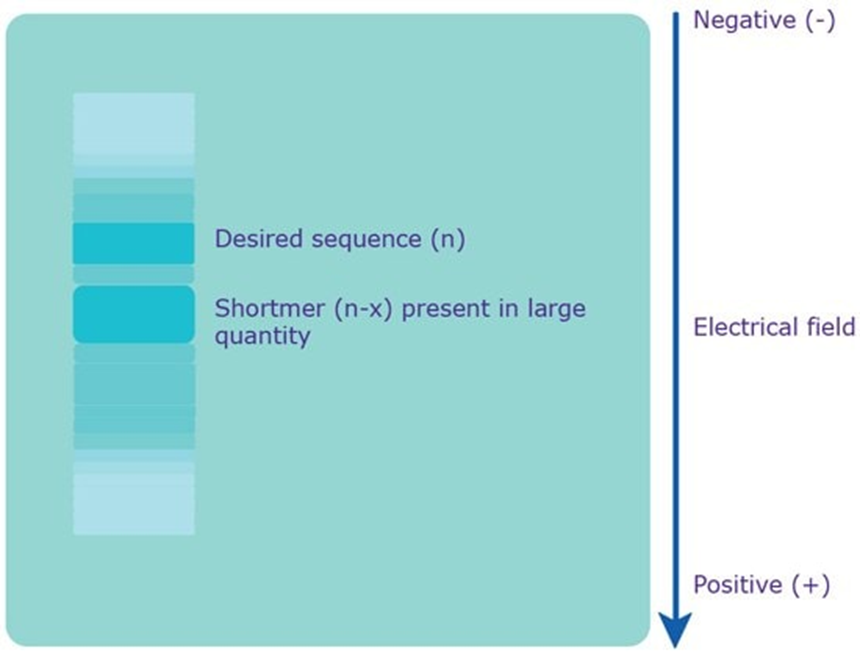
Sắc ký lỏng hiệu suất cao trao đổi ion (IE-HPLC) (cụ thể là trao đổi anion) dựa trên số lượng nhóm tích điện âm của nhóm phosphate trong khung xương chính của oligonucleotide. Phương pháp trao đổi anion liên quan đến việc sử dụng các pha động có nồng độ muối cao như Nacl trên các cột có chứa các pha tĩnh amoni. Các trình tự lỗi có kích thước ngắn (shortmer) thường có số lượng điện tích âm ít hơn so với trình tự mục tiêu do đó các trình tự lỗi thường có liên kết yếu với cột nên được rửa giải sớm hơn so với trình tự mục tiêu (hình 4). Tuy nhiên, IE-HPLC bị giới hạn bởi độ dài, thường khoảng 40 bases. Các oligonucleotide dài hơn dẫn đến khả năng phân tách thấp hơn giữa trình tự mục tiêu và trình tự lỗi; và do đó, độ tinh khiết thường thấp hơn và kém nhất quán hơn.
Lý do chính để sử dụng IE-HPLC thay vì RP-HPLC là để tinh chế các oligonucleotide có mang các cấu trúc thứ cấp phức tạp, thường được tìm thấy trong các trình tự có hàm lượng GC cao. IE-HPLC có hiệu quả đối với các oligonucleotide như vậy vì pha động có độ pH cao, làm đứt gãy các liên kết hydro và do đó, phá vỡ cấu trúc thứ cấp. Kỹ thuật IE-HPLC này có thể được thực hiện sau quá trình tinh sạch RP-HPLC để tăng độ tinh khiết của sản phẩm oligo.
Phương pháp điện di gel polyacrylamide (PAGE)
Điện di gel polyacrylamide (PAGE) sử dụng môi trường biến tính cụ thể là môi trường có chứa URE (URE PAGE) để phân các oligonucleotide dựa trên trọng lượng phân tử thay vì điện tích. Trong điều kiện thích hợp, các oligonucleotide khác nhau bởi 1 nucleotide duy nhất có thể được phân tách. Khả năng phân tách kích thước hiệu quả này thường mang lại mức độ tinh khiết cao nhất có thể đạt được trong bất kỳ phương pháp tinh sạch nào hiện có. Hiệu suất thu hồi mục tiêu từ kỹ thuật PAGE thường thấp hơn so với các phương pháp khác do khả năng loại bỏ trình tự lỗi và cũng như quy trình phức tạp để phân tách được các oligonucleotide mục tiêu. PAGE thường được khuyến nghị khi cần các sản phẩm có độ tinh khiết cao để ứng dụng trong các thí nghiệm yêu cầu độ chính xác cao và đối với các trình tự có chiều dài lớn hơn ≥ 60 bazơ. Các sản phẩm sau khi tinh sạch bằng PAGE thường có độ tinh khiết cao >95%.
TÀI LIỆU THAM KHẢO
- Oligonucleotide purification methods for your research – UK. (n.d.). Retrieved January 8, 2025, from https://www.thermofisher.com/vn/en/home/brands/thermo-scientific/molecular-biology/molecular-biology-learning-center/molecular-biology-resource-library/spotlight-articles/oligonucleotide-purification-methods.html
- (N.d.). Sigmaaldrich.com. Retrieved January 8, 2025, from https://www.sigmaaldrich.com/VN/en/technical-documents/technical-article/genomics/dna-and-rna-purification/best-purification





